Когда мы смотрим на мир вокруг нас, мы видим только малую часть того, что действительно происходит. Возможно, вы заметили, как химические реакции протекают перед вашими глазами, но сложно понять, как это происходит и почему. Суть дела в том, что они основываются на неуловимых силах, которые взаимодействуют на самом малом уровне - на уровне молекул.
Молекулы, иногда называемые "строительными блоками" живого и не живого мира, на самом деле являются сложными сущностями. Внутри каждой молекулы скрыты атомы, которые в свою очередь обладают субатомными частицами - электронами, про ядра которых мы все учили в школе. Однако редко задумываемся о том, что происходит с этими электронами, когда две молекулы вступают в химическую реакцию.
Оказывается, электроны имеют свободу перемещаться вокруг ядер и занимать определенные позиции, называемые орбиталями. Эти орбитали представляют собой своего рода "облака", в которых электроны могут находиться в разное время. Как расположены эти орбитали, между какими атомами они располагаются и как они взаимодействуют - все это влияет на процессы реакции и ее результаты.
Основные принципы взаимодействия с орбиталями в химических процессах

В данном разделе мы рассмотрим основные принципы и подходы, необходимые для эффективного взаимодействия с орбиталями в процессах химических превращений. В химии, как и в жизни, удачное взаимодействие совершается на основе особых принципов и правил, которые позволяют трогать сердца атомов и молекул, будоражить их электронные облака и создавать новые вещества.
Для того, чтобы взаимодействовать с орбиталями, необходимо соблюдать определенные правила подбора и учета энергетических уровней. Орбитали, будучи своего рода ареной для химических реакций, имеют различные энергетические уровни, которые нужно учитывать при выборе соответствующих молекул для взаимодействия. Понимание и учет энергетических принципов позволяют эффективно проектировать и проводить химические реакции, получая желаемые продукты превращений.
Кроме того, не менее важным аспектом является наличие правильной геометрической ориентации для успешного взаимодействия орбиталей. Молекулы имеют определенные пространственные конфигурации, и понимание их геометрии играет ключевую роль в определении эффективности химической реакции. Взаимодействие орбиталей происходит посредством перекрытия, и правильное сочетание орбиталей с нужными геометрическими параметрами становится залогом успешной реакции.
Таким образом, в данном разделе мы рассмотрим основные принципы работы с орбиталями в химических процессах, включая энергетические уровни и геометрическую ориентацию. Понимание и применение этих принципов позволяют достичь желаемых результатов в химическом синтезе и разработке новых веществ и материалов.
Виды орбиталей и их роль в химических процессах

Разнообразность орбиталей и их взаимодействие играют важную роль в проведении химических реакций. Различные типы орбиталей демонстрируют разные свойства и возможности, которые могут быть использованы в процессе образования и разрушения химических связей. Они представляют собой фундаментальные концепции, позволяющие понять, как происходят реакции между атомами и молекулами.
Подобно строительным блокам, орбитали могут быть классифицированы по своей форме и ориентации в пространстве. К этим формам относятся s-, p-, d- и f-орбитали, каждая из которых обладает своими особенностями и возможностями в реакциях. Орбитали s-типа имеют форму сферы, p-орбитали выглядят как две щупальца, d-орбитали имеют форму чашки, а f-орбитали выглядят сложнее и более уникально.
Знание различных типов орбиталей помогает понять, какие элементы и соединения могут образовывать сильные и слабые химические связи, а также как наличие или отсутствие конкретной орбитали может повлиять на стабильность молекулы. Например, электроны, находящиеся в s-подуровне, могут участвовать в образовании ковалентных связей, в то время как электроны в d-подуровне могут быть активными в реакциях окисления-восстановления.
Важным моментом является также взаимодействие орбиталей разных атомов или групп атомов в процессе химических реакций. Правильное сочетание орбиталей и их перекрытие может приводить к формированию новых связей и созданию сложных молекул. Взаимодействие орбиталей также может вызывать изменение орбиталей соседних атомов и, следовательно, изменение их химической активности.
Необходимость понимания роли и свойств различных орбиталей в химических процессах заключается в том, чтобы предсказать, какие реакции будут возможны и каким образом они могут протекать. Таким образом, изучение видов орбиталей помогает расширить наши знания о химической реакционной способности веществ и создать новые материалы и соединения с нужными свойствами.
Взаимосвязь строения атомов и молекул с особенностями орбиталей
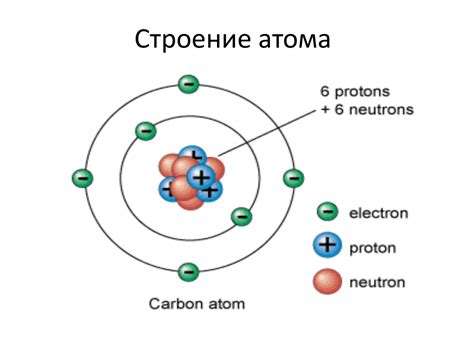
В данном разделе мы рассмотрим важные аспекты, связанные со строением атомов и молекул, которые оказывают влияние на свойства и поведение орбиталей. Орбитали служат основной моделью для объяснения разнообразных химических явлений и процессов, и их свойства напрямую зависят от характеристик атомов и молекул.
- Структура атома: Взаимное расположение электронов в атоме играет ключевую роль в формировании орбиталей. Орбитали различаются по форме, ориентации и размеру, что объясняется электронной структурой атома и его энергетическим уровнем.
- Химическая связь: Взаимодействие между атомами, в результате которого образуются молекулы, определяет свойства орбиталей. Различные типы химических связей, такие как ковалентные и ионные связи, влияют на структуру орбиталей и их способность вступать в реакции.
- Энергетические уровни электронов: Распределение электронов по энергетическим уровням атома и молекулы имеет прямое отношение к конфигурации орбиталей. Энергетические уровни определяют возможность электронов занимать определенные орбитали и участвовать в химических реакциях.
- Молекулярная геометрия: Расположение атомов в пространстве, в свою очередь, влияет на форму и ориентацию орбиталей, определяя их вероятность нахождения электронов внутри молекулы и их реакционную активность.
Взаимодействие квантовой механики и орбиталей в химических реакциях

Квантовая механика – это физическая теория, которая описывает поведение частиц на микроскопическом уровне. Она позволяет рассчитать вероятность того, что частица находится в определенном месте или состоянии. Одним из ключевых принципов квантовой механики является принцип неопределенности, который утверждает, что невозможно одновременно точно измерить положение и скорость частицы.
Орбитали, с другой стороны, представляют собой области пространства, в которых электроны могут находиться со значительной вероятностью. Они различаются по форме и энергии, и могут быть представлены в виде трехмерного графика, называемого электронной оболочкой. Интересно, что форма и распределение орбиталей вокруг атома определяют его химические свойства и способность к образованию химических связей.
В химических реакциях, квантовая механика и орбитали становятся главными игроками. Она позволяет рассчитать энергию, которая расходуется на разрыв и образование химических связей, а также предсказать вероятность того, что реакция произойдет. Орбитали, в свою очередь, определяют химическую активность атомов и молекул, а также их способность объединяться в новые соединения.
Исследование взаимодействия квантовой механики и орбиталей в химических реакциях открывает новые горизонты в понимании и прогнозировании химических процессов. При помощи этих знаний мы можем разрабатывать новые материалы, обеспечивать устойчивую экологию и создавать инновационные технологии.
Методы формирования и получения орбиталей

Первым методом, который мы рассмотрим, является метод квантовой механики. Квантовая механика - это физическая теория, которая описывает поведение мельчайших частиц, включая электроны. Она позволяет определить возможные состояния электрона вокруг ядра и формировать соответствующие орбитали.
Другим методом является метод математического моделирования. При помощи математических алгоритмов и вычислительных программ исследователи могут создавать модели орбиталей на основе определенных параметров. Это позволяет предсказывать структуру и свойства молекул без необходимости выполнения физических экспериментов.
Также существуют различные экспериментальные методы, которые позволяют получать орбитали в действительности. Например, методом рентгеноструктурного анализа можно определить расположение атомов в молекуле и, следовательно, орбиталей электронов.
- Метод квантовой механики
- Метод математического моделирования
- Экспериментальные методы, включая рентгеноструктурный анализ
Понимание методов создания и получения орбиталей является важным шагом в изучении химии и позволяет углубить наши знания о строении и свойствах веществ.
Современные подходы и методы исследования орбиталей: открытие новых горизонтов в изучении химической структуры и взаимодействий
В настоящее время существует широкий спектр инструментов и технологий, которые позволяют исследовать орбитали, основные строительные блоки химических реакций. Эти инструменты и технологии позволяют углубить наше понимание молекулярных взаимодействий, реакционных механизмов и предсказывать химические свойства веществ.
Одним из самых мощных методов для изучения орбиталей является теоретический подход, основанный на квантовой механике. С помощью квантово-механических расчетов можно получить информацию о распределении электронной плотности в молекулах и орбитальных энергиях. Уникальность этого подхода заключается в возможности предсказывать и объяснять свойства веществ на основе их электронной структуры.
В последние годы наблюдается растущий интерес к разработке новых методов визуализации и визуальной анализа орбиталей. С помощью современных программных пакетов и инструментов можно строить трехмерные модели молекул и их орбиталей, изучать их геометрическую форму, поискать симметричные элементы и проводить детальные сравнения различных образцов. Визуализация орбиталей позволяет наглядно представить их поведение в химических реакциях, а также взаимодействие с другими молекулами.
Еще одним захватывающим направлением в исследовании орбиталей является применение современных методов спектроскопии. С помощью спектроскопических методов можно наблюдать и анализировать энергетические уровни электронов в молекулах, а также их переходы между этими уровнями. Такие методы, как электронная спектроскопия и ядерный магнитный резонанс (ЯМР) спектроскопия, предоставляют множество информации о структуре молекул, включая орбитальные энергии, заселенность орбиталей и взаимодействия с другими частицами.
Современные инструменты и технологии для изучения орбиталей играют важную роль в прогрессе и развитии химии и науки в целом. Их применение открывает новые возможности для глубокого понимания химических структур и процессов, а также помогает разрабатывать новые материалы и лекарственные препараты. Благодаря развитию этих инструментов и технологий, научное сообщество продолжает расширять свои знания о мире молекул и их реакций, открывая перед нами новые горизонты возможностей и применений.
Влияние энергии орбиталей на активность веществ в химических реакциях
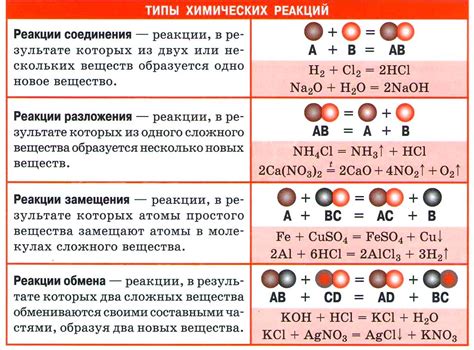
Различные орбитали обладают разной энергией и формой, что определяет их способность принимать и отдавать электроны при химических реакциях. Некоторые орбитали имеют высокую энергию и могут легко принимать дополнительные электроны, что делает их активными веществами среди других. Другие орбитали, напротив, имеют низкую энергию и могут отдавать свои электроны другим веществам. Такое различие в энергии орбиталей является определяющим фактором для процессов химической активности.
Важно отметить, что энергия орбиталей может быть изменена различными способами, такими как влияние внешних факторов, включая температуру и давление, а также изменение структуры молекулы. Например, при изменении электронной конфигурации атома изменяется энергия его орбиталей, что в свою очередь влияет на его реакционную способность. Это делает возможным контроль и регулирование химической активности веществ через манипуляцию энергией и распределением орбиталей.
| Влияние орбиталей на химическую активность: |
|---|
| Различия в энергии орбиталей |
| Принятие и отдача электронов |
| Изменение энергии орбиталей под воздействием внешних факторов |
| Манипуляция энергией и распределением орбиталей для контроля активности |
Роль орбиталей в катализе и их применение в реакциях
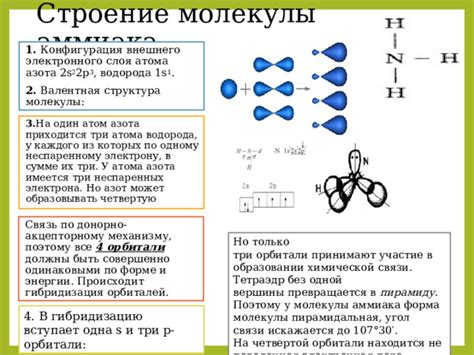
Перед нами открывается захватывающая область, в которой орбитали играют важную роль в сфере катализа и проявляют свои уникальные свойства в ходе разнообразных реакций. Через активное участие орбиталей образуются промежуточные состояния, облегчающие прохождение реакций и ускоряющие превращение реагентов в продукты. Уникальные свойства орбиталей позволяют им эффективно взаимодействовать с реагентами и обеспечивают проявление катализаторов в определенных реакциях.
Катализаторы, основанные на орбиталях, обладают способностью проводить энергетические переходы без участия фазы (вещества) исходной реакции, что способствует повышению эффективности реакций и сокращению стадий процесса.
Координационная химия активно использует орбитали для образования связей между каталитическими частицами и реагентами, что позволяет повышать скорость реакции и улучшать выход целевых продуктов.
Орбитали также применяются в реакциях дегидрирования и гидрации, обеспечивая эффективный перенос водорода в реакционную среду, что повышает конверсию реагентов и селективность процесса.
В сфере органического синтеза орбитали особенно полезны при проведении катализируемых реакций, где они позволяют управлять стереохимией и получать продукты с определенными конфигурациями.
Рабочая сфера орбиталей в катализе является обширной и постоянно развивающейся. Понимание и применение их свойств в реакциях является важной задачей для достижения более эффективных и экологически чистых процессов.
Применение орбиталей в органической химии и синтезе органических соединений
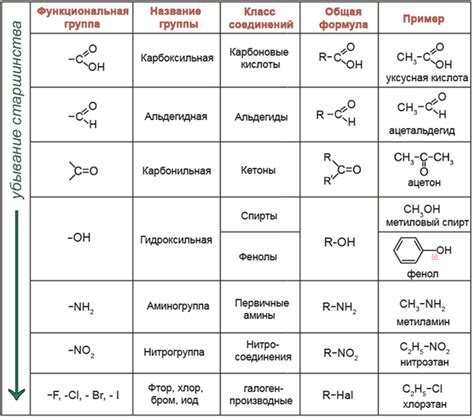
Различные орбитали играют важную роль в органической химии и синтезе органических соединений. Они представляют собой пространственные области вокруг атомов, где находятся электроны. Орбитали определяют возможности взаимодействия и реакционные способности атомов и молекул.
Орбитали в органической химии могут быть использованы для предсказания химической активности молекул, структурной стабильности и реакционных механизмов. Использование орбиталей позволяет установить взаимосвязь между электронным строением молекулы и ее химическими свойствами.
Одним из применений орбиталей является определение положения и реакционных способностей функциональных групп в органической молекуле. Определение позиции и возможности реакции функциональных групп позволяет предсказывать химические превращения и свойства соединений.
- Орбитали также играют важную роль в синтезе органических соединений. На основе знания электронной структуры атомов и молекул и возможности взаимодействия орбиталей, органические соединения могут быть спроектированы и синтезированы с целевыми свойствами и функциями.
- Кроме того, орбитали позволяют понять и предсказать реакционные механизмы, которые происходят между органическими соединениями. Изучение орбиталей и электронной структуры может помочь установить последовательность шагов и стагнирование реакций, что позволяет эффективно контролировать синтез и модификацию органических молекул.
- Орбитали также находят применение в изучении электронных переходов, связанных с оптической активностью органических соединений. Анализ орбиталей позволяет предсказать видимый и ультрафиолетовый спектры соединений, что важно для определения их структуры и идентификации.
В заключении, применение орбиталей в органической химии и синтезе органических соединений играет ключевую роль в понимании и предсказании свойств молекул, контроле реакций и дизайне новых соединений с целевыми свойствами.
Перспективы исследования энергетических уровней и их влияние на химические превращения
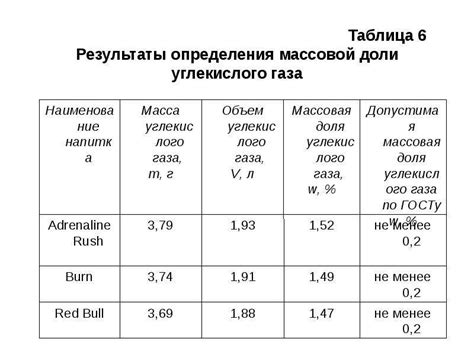
Благодаря постоянному развитию экспериментальных и вычислительных методов, исследователи получают все больше информации о строении и энергетических состояниях молекул и ионов. Современные методы спектроскопии, масс-спектрометрии и квантово-химические расчеты позволяют определить положение энергетических уровней и их зависимость от взаимодействия атомов и молекул. Это открывает перед исследователями возможность проследить динамику процессов на молекулярном уровне и предсказать результаты химических реакций.
Исследование энергетических уровней имеет широкие перспективы для применения в различных областях химии. На основе полученных данных можно рассчитать кинетические параметры химических реакций, определить оптимальные условия для проведения синтеза новых соединений и улучшить существующие процессы. Понимание энергетических уровней и механизмов реакций также позволяет улучшить эффективность энергетических систем и разработать новые методы защиты окружающей среды.
- Изучение влияния энергетических уровней на реакционные механизмы
- Применение полученных данных в синтезе новых веществ и материалов
- Кинетические исследования и оптимизация химических процессов
- Разработка новых методов защиты окружающей среды и энергосберегающих технологий
Вопрос-ответ

Какие орбитали существуют в химических реакциях?
В химических реакциях существуют различные типы орбиталей, такие как s-, p-, d- и f- орбитали. Они различаются по форме и энергетическому уровню.
Какие принципы лежат в основе создания орбиталей в химических реакциях?
Создание орбиталей в химических реакциях основано на принципах квантовой механики. Одним из таких принципов является принцип запрещения Паули, гласящий, что каждая орбиталь может быть занята не более чем двумя электронами с противоположным спином.
Какие свойства орбиталей влияют на процессы химических реакций?
Свойства орбиталей, такие как их форма, размер, энергетический уровень и заполнение электронами, влияют на процессы химических реакций. Например, форма орбиталей может влиять на вероятность их взаимодействия с другими орбиталями и молекулами, а энергетический уровень - на их реакционную активность.