Ученые всегда стремились понять, как устроен мир вокруг нас. И одним из главных вопросов, которые они задавали себе, было: "Как узнать количество вещества в химической реакции?" Это оказалось сложным заданием, требующим разработки собственных методов и техник.
Научные исследования показывают, что определение количества вещества возможно благодаря использованию различных принципов. Одним из них является принцип массообмена, который основывается на измерении изменения массы вещества до и после реакции. Другим принципом является обратимость реакции, когда известно количество вещества, с которым взаимодействует исследуемое вещество.
Существуют также техники, позволяющие определить количество вещества в химической системе. Одной из таких техник является гравиметрический метод, основанный на измерении массы происходящих реакций. Еще одной техникой является волюметрический метод, который основан на измерении объема газов и жидкостей, участвующих в реакции.
Молярность: значимость и применение в химических расчетах

Одним из принципов определения молярности является использование уравнения реакции, которое позволяет установить соотношение между начальными и конечными веществами в химической реакции. Расчет молярности основывается на изучении массы вещества, его объема и молекулярной массы, что позволяет установить соотношение между числом молей и объемом раствора. Для этого используются различные методы, включая дистилляцию, титрование и гравиметрию.
- Другим методом определения молярности является дистилляция. Этот метод обычно используется для измерения молярности жидкостей. Процесс дистилляции основывается на различии в кипящих точках компонентов смеси и позволяет получить пары и оставить за собой более легкую фракцию. После дистилляции можно рассчитать молярность, исходя из полученного объема и массы продукта.
Молярность является ключевым параметром в химических расчетах, позволяющим определить количество вещества, а также выполнять лабораторные исследования и оценивать результаты реакций. Понимание и использование молярности в химии является неотъемлемой частью широкого спектра химических наук и играет важную роль в практическом применении химических процессов и производств.
Титриметрические подходы в определении количества вещества: принципы и примеры

Титриметрические методы включают в себя широкий спектр техник и процедур, которые применяются для определения концентрации различных веществ в растворе. Они основаны на реакции между исследуемым веществом и определенным реагентом, который добавляется постепенно и измеряется до момента полного окисления, осаждения или нейтрализации исследуемого вещества.
- Активный хлор: Примером титриметрического метода определения количества активного хлора в растворе может быть использование раствора йодида калия (KI) в присутствии крахмала в качестве индикатора. При взаимодействии активного хлора с раствором йодида калия образуется йод, который затем реагирует с крахмалом, образуя синий комплекс. Измерение объема использованного реагента с позиции равновесия позволяет определить количество активного хлора в исследуемом растворе.
- Железо: Определение количества железа в растворе можно осуществить с помощью раствора редокс индикатора, такого как тиоцианат калия (KSCN) и хлорида железа(III) (FeCl3). При добавлении тиоцианата к раствору с железом образуется красное соединение, а точка эквивалентности достигается при полном переходе железа из железа(III) в железо(II). Измерение объема использованного реагента позволяет определить количество железа в исследуемом растворе.
- Кислород: Для определения количества растворенного кислорода в воде может быть использовано растворение растворимого окисла, например, йодида с крахмалом в качестве индикатора. Полное растворение реагента достигается при полном потреблении кислорода, и показателем является изменение цвета реакционной смеси. Количество использованного реагента позволяет определить количество растворенного кислорода в воде.
Метод гравиметрии: измерение массы образца для определения его количество

В гравиметрии применяются различные техники и процедуры для точного измерения массы образца. Одной из ключевых процедур является отвешивание, при котором масса образца определяется с использованием аналитических весов. В результате этого измерения мы получаем точное значение массы образца, которое затем используется для определения количества интересующего нас компонента в веществе.
Процесс гравиметрического определения количества вещества основан на осаждении или выделении интересующего компонента в виде инертного осадка, который затем обрабатывается и измеряется для определения его массы. Этот метод требует аккуратности и тщательной обработки образца, чтобы обеспечить точность результатов.
| Преимущества гравиметрического метода | Ограничения гравиметрического метода |
|---|---|
| Высокая точность и надежность | Длительное время анализа |
| Применяется для различных типов веществ и соединений | Требует наличия достаточного количества образца |
| Не требует сложного оборудования | Чувствительность к внешним воздействиям |
Гравиметрический метод широко применяется в химическом анализе и позволяет получить точные результаты определения количества вещества. Его преимущества и ограничения должны быть учтены при выборе метода анализа в конкретных исследованиях.
Спектроскопия: применение поглощения или испускания электромагнитного излучения для количественного анализа
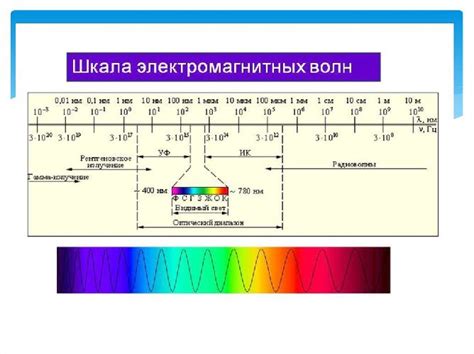
Основной принцип спектроскопии заключается в том, что каждое вещество имеет уникальный спектральный отпечаток, связанный с его структурой и энергетическими уровнями. При взаимодействии с электромагнитным излучением, вещество может поглотить или испустить определенные длины волн, что обуславливает его цвет или спектральные полосы на спектрограмме.
Существует несколько основных техник спектроскопии, таких как атомно-абсорбционная спектроскопия, флуоресцентная спектроскопия, инфракрасная спектроскопия и ультрафиолетовая видимая спектроскопия. В каждой из этих техник используется различный диапазон электромагнитного излучения для анализа разных типов веществ.
- Атомно-абсорбционная спектроскопия основана на измерении поглощения света атомами вещества.
- Флуоресцентная спектроскопия изучает испускание света атомами или молекулами, возбужденными воздействием электромагнитного излучения.
- Инфракрасная спектроскопия использует поглощение инфракрасного излучения веществом, позволяя исследовать его внутреннюю структуру и связи.
- Ультрафиолетовая и видимая спектроскопия используют поглощение и испускание света в ультрафиолетовом и видимом диапазонах, чтобы определить концентрацию вещества.
Использование спектроскопии в количественном анализе позволяет получить точные и надежные данные о содержании вещества в образце. Этот метод является универсальным и предоставляет возможность изучать различные типы веществ в широком спектре областей наук и технологий.
Хроматографические методы: расщепление смесей и определение объема вещества
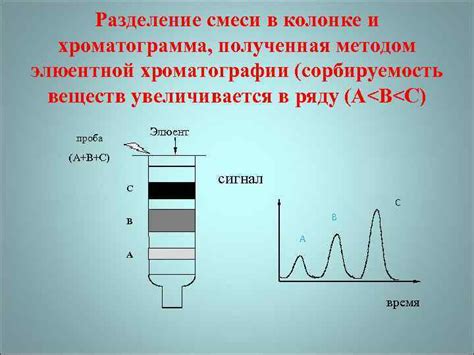
- Селективное расщепление: хроматографические методы основаны на принципе различной взаимодействия компонентов смеси с стационарной и подвижной фазами. Это позволяет эффективно разделить смесь на отдельные компоненты.
- Жидкостная хроматография: один из распространенных видов хроматографии, где подвижной фазой является жидкость, а стационарной - твердое или жидкое вещество с поверхностью большой площади. С помощью данного метода можно выделить и определить количества вещества в смеси.
- Газовая хроматография: другой распространенный вид хроматографии, где подвижной фазой является газ, а стационарной - твердое или жидкое вещество с поверхностью большой площади. Этот метод эффективен для разделения и определения газообразных и летучих веществ.
- Тонкослойная хроматография: метод, основанный на разделении смеси на слабо взаимодействующие компоненты посредством проведения ее через тонкий слой стационарной фазы на подложке. Этот метод широко применяется для обнаружения и определения различных веществ в образцах.
Хроматографические методы являются мощным инструментом в химическом анализе, позволяющим не только разделить смеси на компоненты, но и определить их количество. Использование различных типов хроматографии позволяет достичь точных результатов и применять эти методы в различных областях науки и промышленности.
Электрохимические методы: применение потенциала и тока для измерения объема вещества

Используя эти методы, можно определить количество вещества, проанализировав изменение показателей электрохимической ячейки. При этом, изменение потенциала и тока является показателем количества вещества, которое участвует в химической реакции.
Основной принцип электрохимических методов заключается в том, что при прохождении электрического тока через раствор или электрохимическую систему, происходят химические реакции. При этом, изменение потенциала и тока можно измерить и использовать для определения количества вещества.
Измерение тока также является эффективным методом определения количества вещества. При прохождении электрического тока через раствор, величина тока зависит от концентрации растворенного вещества. Следовательно, измерение тока позволяет определить количество вещества, участвующего в электрохимической процессе.
Электрохимические методы широко применяются в области аналитической химии, где точность и надежность определения количества вещества является критически важным. Они позволяют проводить анализ различных образцов с высокой чувствительностью и точностью.
Измерение отношения массы к заряду для определения количества вещества с использованием масс-спектрометрии

Масс-спектрометрия представляет собой мощный метод анализа в химии, основанный на измерении отношения массы к заряду (m/z) для определения количества вещества. Этот метод позволяет получить информацию о массе молекулы, ее составе и структуре, а также о количестве присутствующего вещества.
Принцип работы масс-спектрометрии основан на разделении ионов в магнитном поле в зависимости от их масс-зарядового отношения. В процессе анализа образец вещества подвергается ионизации, в результате чего образуются положительные или отрицательные ионы. Затем ионы ускоряются и проходят через магнитное поле, которое отклоняет их траекторию в зависимости от их массы и заряда.
Масс-спектрометрия позволяет определить количественное содержание вещества в образце. С помощью этого метода можно измерять массу отдельных атомов, молекул и их фрагментов. Благодаря современным технологиям, масс-спектрометрия является достаточно точным и чувствительным методом анализа, который находит широкое применение в разных областях химии.
Фотометрия: измерение светового потока или его интенсивности для определения количества вещества
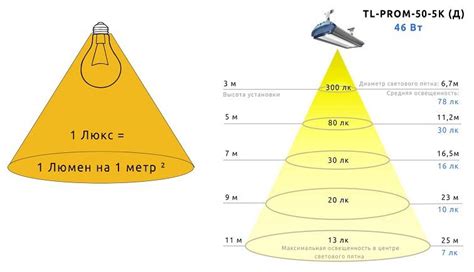
Фотометрический анализ позволяет определить, сколько вещества содержится в рассматриваемой пробе путем измерения света, проходящего через нее. Для этого используются фотометры, спектрофотометры и другие приборы, которые измеряют интенсивность света в определенном спектральном диапазоне.
Измерение светового потока или интенсивности света позволяет получить количественные данные о содержании вещества в анализируемой пробе. Эти методы широко применяются в химическом анализе для определения концентрации растворов, содержания вредных веществ в окружающей среде, а также для контроля качества исследуемых материалов.
Вопрос-ответ

Какие основные принципы лежат в основе методов определения количества вещества в химии?
Основными принципами методов определения количества вещества в химии являются точность, выборочность и чувствительность. Точность обеспечивается путем использования калибровочных стандартов и повторяемости эксперимента. Выборочность позволяет определить нужное вещество в смеси, отделив его от других компонентов. Чувствительность зависит от способности метода обнаружить и измерить даже малые количества вещества.
Какие техники используются для определения количества вещества в химии?
Для определения количества вещества в химии используются различные техники, включая гравиметрические, титриметрические, спектрофотометрические, электроаналитические и хроматографические методы. Гравиметрические методы основаны на измерении массы вещества, титриметрические - на реакции, в результате которой происходит образование химического соединения. Спектрофотометрические методы регистрируют поглощение или поглощение электромагнитного излучения веществом, а электроаналитические определяют количественное содержание вещества с использованием электрохимических методов.
Как проводится гравиметрический метод определения количества вещества?
Гравиметрический метод определения количества вещества основан на измерении массы вещества. Для этого первоначально измеряют массу образца с неизвестным количеством вещества, затем производят реакцию, в результате которой образуется химическое соединение с известным составом. После окончания реакции измеряют массу образца химического соединения и рассчитывают массу исходного вещества с использованием стехиометрии реакции.
Как работают электроаналитические методы определения количества вещества?
Электроаналитические методы определения количества вещества используют электрохимические методы для определения количества вещества. Например, в методе поляризации проводят измерение изменения потенциала электрода при добавлении раствора исследуемого вещества. По полученным данным рассчитывают содержание вещества в растворе. Другой пример - метод кулонометрии, где определение количества вещества основано на измерении заряда, проходящего через раствор в процессе электролиза.
Какие существуют основные принципы и техники определения количества вещества в химии?
Основные принципы и техники определения количества вещества в химии включают: использование химических реакций с известными реагентами, гравиметрические методы, ведение количественного анализа, спектрометрические методы, электрохимические методы и титриметрические методы. Каждая из этих техник имеет свои преимущества и ограничения, но в сочетании они позволяют определять количество вещества с высокой точностью.
Какие методы относятся к спектрометрическим методам определения количества вещества?
Спектрометрические методы определения количества вещества включают спектрофотометрию, флуориметрию, атомно-абсорбционную спектрометрию и инфракрасную спектроскопию. Эти методы основаны на измерении светового поглощения или испускания веществами при взаимодействии с электромагнитным излучением определенной длины волны. Спектрометрические методы обладают высокой чувствительностью и позволяют определять количество вещества в крайне малых концентрациях.



